时间:2020-06-04 09:42 │ 来源:医药云端工作室 │ 阅读:1459
近日,国家药监局批准了多个新药上市申请。包括:
百济神州的“泽布替尼胶囊”,首个获批的国产BTK抑制剂
恒瑞、扬子江的“吉非替尼片”,国家集采品种,销售额超20亿元
Genzyme的“注射用拉罗尼酶浓溶液获批上市”,第二批临床急需境外上市药品目录药品。
据悉,泽布替尼用于治疗MCL的适应症已于2019年11月14日获得FDA加速批准,商品名为Brukinsa。目前,泽布替尼该适应症也已经在以色列提交上市申请,泽布替尼在以色列的商业化权益已经授权给Medison公司。2020年第一季度,泽布替尼在美国的销售额为72万美元。
泽布替尼是全球第3款获批上市的BTK抑制剂,也是国内获批的第2款BTK抑制剂。另外,诺诚健华的奥布替尼也已经在中国申报上市,有望成为第3款在中国上市的BTK抑制剂。
赛诺菲:罕见病用药“注射用拉罗尼酶浓溶液”获批上市
恒瑞、扬子江“吉非替尼片”获批上市,六强争霸赛开启
近日,国家药监局官网显示,恒瑞医药和扬子江药业的吉非替尼片上市申请均获得批准,两企业均按照4类申请,获批后视同通过一致性评价。


吉非替尼是一种选择性表皮生长因子受体酪氨酸激酶抑制剂,适用于表皮生长因子受体基因具有敏感突变的局部晚期或转移性非小细胞肺癌患者的一线治疗,及适用于治疗既往接受过化学治疗的局部晚期或转移性非小细胞肺癌患者。
吉非替尼直接抑制肿瘤生成的靶点,使肿瘤细胞特异性死亡而不波及正常细胞组织;与传统化疗药物相比,吉非替尼在取得抗肿瘤疗效的同时较少引起患者全身性副反应。此外,吉非替尼片是口服剂,接受其治疗的患者无须住院给药,这很大程度上提高了患者及其家属的生活质量。
吉非替尼临床应用广泛,目前已被《NCCN非小细胞肺癌临床实践指南(2020.V1)》、《中国临床肿瘤学会(CSCO)原发性肺癌诊疗指南(2019)》等指南推荐作为EGFR突变非小细胞肺癌患者的一线治疗药物,且已进入2019年国家乙类医保和2018年国家基药目录。
吉非替尼2002年7月在日本首次上市,2003年5月获FDA批准在美国上市,2005年,原研药企阿斯利康的吉非替尼片(易瑞沙)在国内上市,并保持国内市场垄断长达11年之久,价格始终高达5000元/盒。
根据医药云端工作室统计,截止目前,该药品已5家企业过评。除此次获批的两家企业外,还有齐鲁制药、科伦制药和正大天晴三家仿制药企业。加上原研企业阿斯利康,六强争霸赛开启。
另据Insight 数据库显示,目前还有南京优科、天士力、上海创诺、苏州特瑞等 7 家企业的仿制药在报上市,其中包括 NATCO 制药公司的进口仿制药,竞争可谓异常激烈。
据米内网数据显示,2018年中国公立医疗机构终端吉非替尼的销售额超过23亿元。目前市场的领军企业为阿斯利康,不过齐鲁制药(海南)的产品至获批上市后一直蚕食原研的份额。
2019阿斯利康市场下降至74.96%,齐鲁制药的市场增长至23.56%,而正大天晴夺得1.48%的市场份额。
6月1日,杭州民生滨江制药有限公司的阿仑膦酸钠片上市申请获得国家药监局批准,该药品按新4类申报,视同通过一致性评价,且为全国首家过评的企业。


仑膦酸钠片,原研厂家为默沙东,主要适用于绝经后妇女骨质疏松症,以预防髋部和脊柱骨折(椎骨压缩性骨折);治疗男性骨质疏松以增加骨量。阿仑膦酸钠片是首个获得FDA批准用于治疗绝经后骨质疏松症的双膦酸盐类药物,也是第一个被美国FDA批准用于治疗男性骨质疏松症的药物。
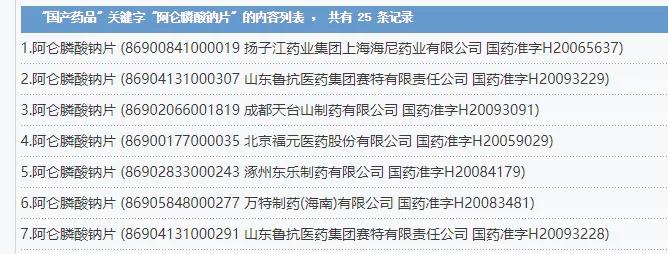
在双磷酸盐制剂中,阿仑膦酸钠片规模并不算大,远不及一众唑来膦酸注射剂的市场规模。 经查询国家药监局网站,该药品目前国内有25个批文号,涉及石药欧意、扬子江上海海尼药业等19家企业,据悉目前除杭州民生滨江制药外,无其他企业申报一致性。