


时间:2020-10-30 16:32 │ 来源:药筛 │ 阅读:1355
这意味着,注射剂一致性评价补充申请通道已经打开。
2018年4月19日,江苏迪赛诺制药申报了盐酸拉贝洛尔注射液的一致性评价补充申请,算是首个正式申请。
然而,由于审评审批的流程、办法以及技术要求等方面不完善、不明确等原因,两年多来,一直没有补充申请获批。
截至月底,已有962个注射剂一致性评价补充申请。其中,有多个品种竞争激烈,多家企业申报,这些申请很有可能集中获批,对于早些申报的企业来说,已丧失早申报的时间优势。
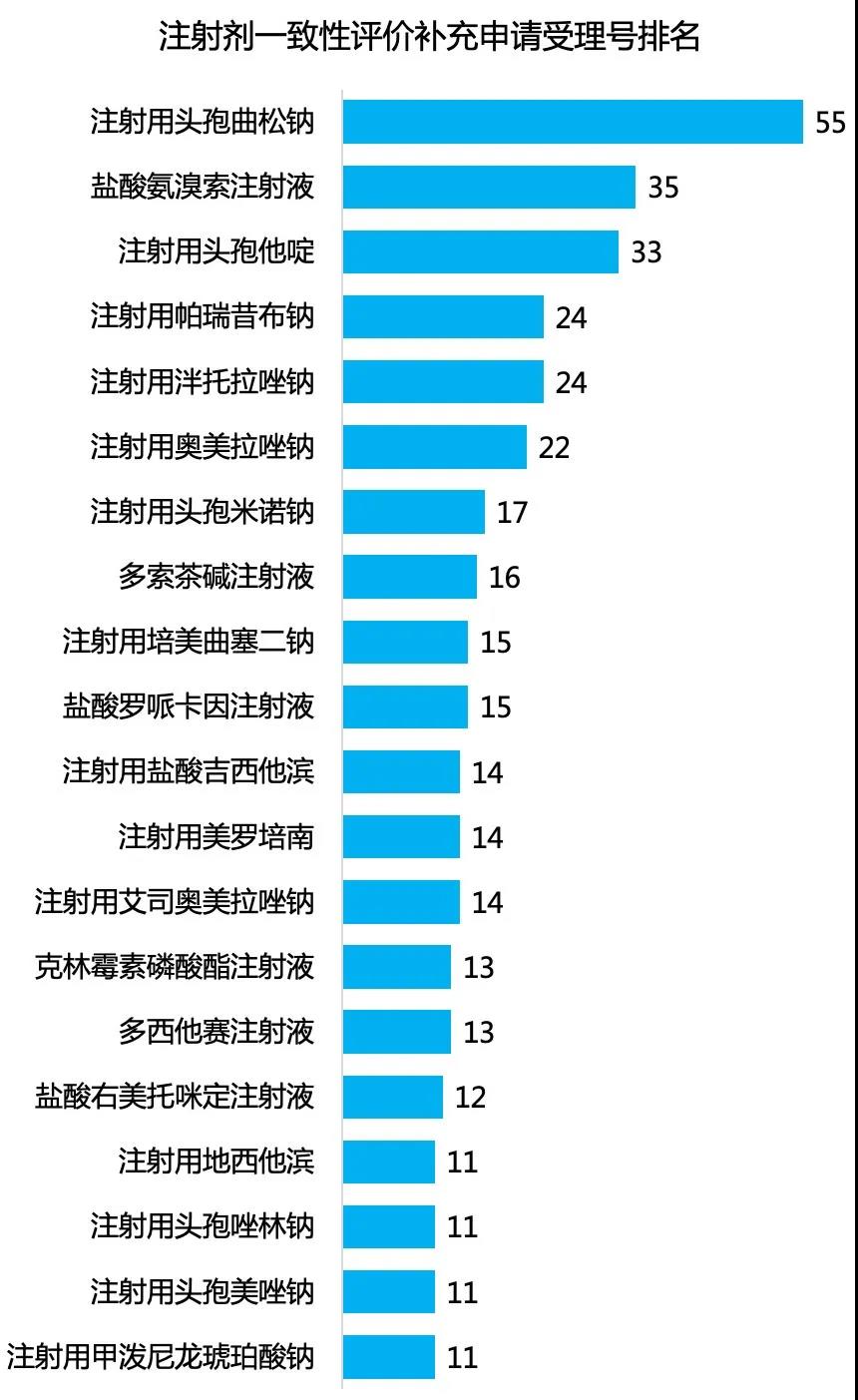
科伦、齐鲁、恒瑞、正大天晴等企业,在申报数量上遥遥领先,重点品种都已申报。
| 企业 | 受理号数 |
| 四川科伦 | 60 |
| 齐鲁制药 | 50 |
| 扬子江药业 | 42 |
| 正大天晴药业集团 | 38 |
| 江苏恒瑞医药 | 27 |
共有42个补充申请受理号的审评状态是“制证完毕”,其中,有一部分已明确不批准,如扬子江药业的依达拉奉注射液(CYHB1950588),正大天晴的盐酸帕洛诺司琼注射液(CYHB1940035、7)等,有一部分受理号虽结论不明确,但从状态时间推测,实际结果也是不批准。
| 药品名称 | 企业 | 结论 | 受理号 |
| 依达拉奉注射液 | 扬子江药业集团南京海陵药业有限公司 | 不批准 | CYHB1950588 |
| 盐酸帕洛诺司琼注射液 | 正大天晴药业集团股份有限公司 | 不批准 | CYHB1940037 |
| 盐酸帕洛诺司琼注射液 | 正大天晴药业集团股份有限公司 | 不批准 | CYHB1940035 |
| 注射用生长抑素 | 扬子江药业集团有限公司 | 不批准 | CYHB1950503 |
| 钆塞酸二钠注射液 | 正大天晴药业集团股份有限公司 | 不批准 | CYHB1940033 |
| 硫辛酸注射液 | 亚宝药业集团股份有限公司 | 不批准 | CYHB1950381 |
| 依达拉奉注射液 | 吉林省博大制药股份有限公司 | 不批准 | CYHB1950029 |
| 硫辛酸注射液 | 开封制药(集团)有限公司 | 不批准 | CYHB1950024 |
| 注射用谷胱甘肽 | 广州白云山明兴制药有限公司 | 撤回申请 | CYHB1840122 |
至今,已有93个注射剂仿制药批文,按新注册办法申报获批,视同通过一致性评价,个别品种已享受到国家集采红利,也有品种体会到集采的杀伤力。
随着更多补充申请获批,越来越多品种满足国家集采条件,残酷的价格战,已近在咫尺。