最新出台的《“十四五”国民健康规划》明确,将扩大药品和高值医用耗材集中采购范围。第七批国家药品集采相关药品信息填报工作也早已开始,注射剂、脊柱类高值耗材等的集采也在推进。
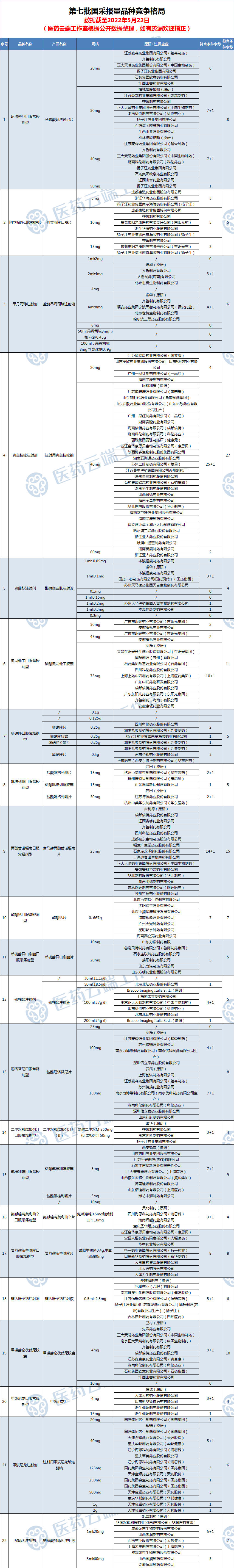
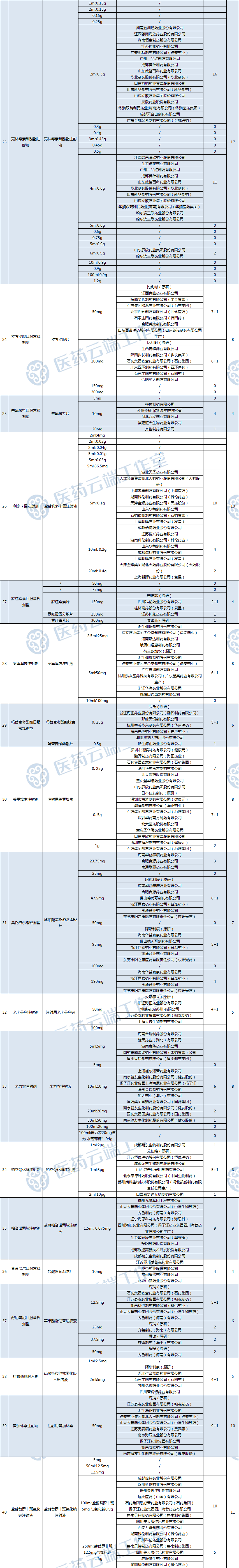
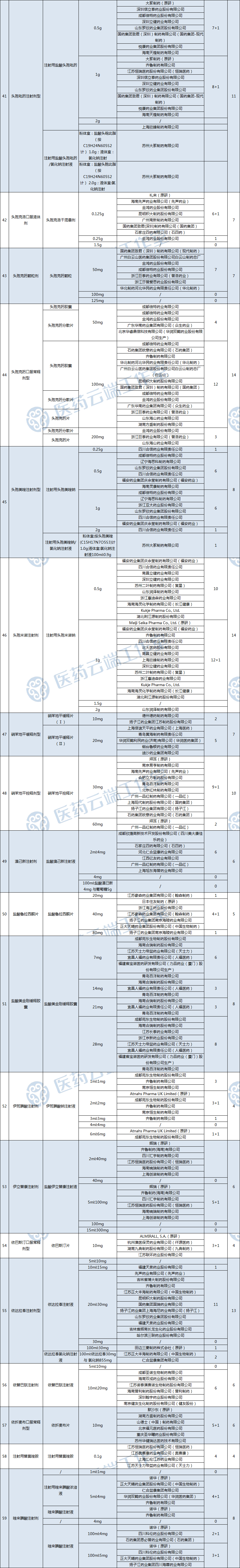
由于疫情的影响,第七批国采从医疗机构启动报量至今,已时隔近3个月。随着各项疫情防控措施的落地实施,6月开始,上海市有望恢复正常生产生活秩序。这也意味着,第七批国采也将在近期会有新动作。根据药事达数据统计,截止5月22日,已有 12个品种竞争企业数量大于等于 10 家。其中,奥美拉唑注射剂竞争最为激烈,已有 26 家企业过评。59个品种共涉及294家企业,其中,齐鲁、扬子江、石药、科伦、中生制药、成都倍特旗下品种均超过10个。(详见文末附表)前5批国采218种药品已落地,涉及766个产品,中选价格平均下降53%5月20日,国务院办公厅印发《“十四五”国民健康规划》,其中提到,完善药品供应保障体系,扩大药品和高值医用耗材集中采购范围,落实集中采购医保资金结余留用政策等。当前,药品集中带量采购改革形成常态化机制,国家集中采购中选药品价格平均下降53%。其中,国家层面组织的药品集采已经开展6批。除第六批国家药品集采为胰岛素专项外,其余均针对化学药。国家组织药品联合采购办公室负责人曾表示,截至今年1月,已开展6批国家组织药品集中采购,其中前5批218种药品已经落地执行,涉及766个产品。在国家层面组织开展药品集中采购的同时,多个地方组成的集采联盟、专项集采也在开展。2021年11月,湖北省医保局发布19省(区、市)集采文件,湖北、河北、山西等联盟地区开展中成药集中带量采购。最终,97家企业的111个产品中选,价格平均降幅为42.27%。根据此次参与集采的联盟地区年度需求量测算,预计每年可节约药品费用超过26亿元。2021年12月,广东省药品交易中心发布关于《广东联盟清开灵等中成药集中带量采购文件》的通知,6省联盟集采,涉及国家基本医保药品目录内用量大、采购金额高的132个药品,覆盖清开灵、复方丹参、连花清瘟等中药临床大品种;2022年5月,《国家组织脊柱类医用耗材集中带量采购方案(征求意见稿)》发布,共纳入13个产品系列,企业将按照产品系列进行竞价。而第七批国采重回化药领域,共涉及阿法替尼、阿立哌唑等59个品种,治疗领域涉及肿瘤、心血管等,其中不乏大品种药物,59个药品中有18个品种市场规模超过10亿元。此次集采还有一大看点,即注射剂品种达到27个,几乎占据集采药品的半壁江山。在此前开展的第五次集采中,注射剂就已经成为“大户”,62个品种中30个为注射剂,占比近半,较前几次集采增加明显。米内网数据显示,2019年全国公立医疗机构化药注射剂的市场规模达到6365亿元。中药领域的集采也在持续开展,除湖北、广东两省牵头的联盟集采外,山西、宁夏、山东也相继组织开展中药饮片集采相关品种采购数据填报等工作。公开数据显示,我国中药饮片加工企业超过1000家,大多数生产企业规模偏小,生产品种多,行业市场集中度低。据《新京报》报道,在北京中医药大学法律系教授邓勇看来,一直以来,中药饮片产品质量良莠不齐,集采有助规范中药饮片质量,有望倒逼企业提升产品质量。随着集采的开展,市场也将实现优胜劣汰,中药饮片产业集中度能得以提高,形成一批有实力、有服务能力的企业。在医用耗材领域,继此前天津联采办先后组织国家人工关节集采、创伤耗材十二省联盟集采后,《国家组织脊柱类医用耗材集中带量采购方案(征求意见稿)》本月发布,脊柱类高值耗材的国家集采根据手术类型、手术部位、入路方式等组建产品系统,共纳入13个产品系列。在高值耗材市场中,骨科植入类医疗器械市场占比达25%,是仅次于血管介入的第二大品类,人工关节、创伤耗材、脊柱类耗材是骨科植入集采的三大重点。据中国药品监督管理研究会发布的《中国医疗器械行业发展报告(2021)》,2020年,国内骨科植入市场规模接近300亿元。其中,脊柱市场市场规模达到89亿元,超过创伤和人工关节。